Загадки химической физики

Ал. Ал. Берлин,
Институт химической физики им. Н.Н. Семенова
Статья опубликована в пятом номере журнала «НБИКС-НТ»
Что такое наука? Каждый человек имеет свой ответ на этот вопрос. Одни считают, что наука – это установление новых законов природы, что встречается чрезвычайно редко. Некоторые думают, что наука – это создание моделей (в том числе математических), описывающих различные явления природы.
Для меня наука состояла в отгадывание загадок, которые задает нам природа. При этом, когда удается наконец решить проблему, другими словами, отгадать эту загадку (или думать, что ты ее отгадал), получаешь удовлетворение (удовольствие), и именно это, я думаю, является главным стимулом заниматься наукой. Во всяком случае для меня. Это фундаментальная наука.
Есть и прикладная наука, цель которой создание новых материалов, веществ, процессов. Везде есть творчество, но разное. В первом случае нас двигает любопытство, во втором — некоторое задание извне.
Впрочем, разделения на фундаментальную и прикладную науку в жизни не происходит. В том смысле, что часто люди, занимающиеся фундаментальной наукой, одновременно делают и какие-то прикладные работы, поскольку фундаментальный результат приводит к необходимости довести его до практики.
С другой стороны выполнение прикладной задачи часто в какой-то момент ведет к возникновению фундаментальной проблемы.
Так изучение практически важных проблем горения – борьба с пожарами, создание двигателей и прочее – привело к теории горения, распространения пламени и т.д. Или чисто фундаментальные ядерные исследования вылились в атомную бомбу. И занимались фундаментальными и прикладными исследованиями одни и те же люди. Конечно, в прикладные работы вовлечено гораздо больше людей и ресурсов. Таких примеров множество.
Приведу несколько примеров таких загадок, встретившихся на моем пути.
- Почему атмосфера земли содержит 21% кислорода?
Возможным ответом является процесс горения лесов (рис. 1).

Рис. 1
Леса увеличивают концентрацию кислорода, а пожары снижают. Ключевым моментом в этом динамическом равновесии являются критические условия горения древесины. При исследовании и сравнении горючести различных материалов пользуются такой характеристикой как «кислородный индекс». Это минимальная концентрация кислорода в подаваемой смеси азот-кислород, при которой поддерживается самостоятельное горение образца материала в определенных стандартных условиях. Удивительным образом для древесины эта величина (~21) совпадает с составом атмосферы земли.
- Как появилась хиральность в живых организмах?
Биологические молекулы (аминокислоты в белках, сахара в ДНК и РНК) во всех живых организмах имеют одну и ту же хиральность, лишь один из двух возможных стереоизомеров, при этом они закручены в одну сторону. Это общее свойство, присущее живым организмам: использовать аминокислоты только одного типа впервые обнаружил великий французский ученый XIX века Луи Пастер.
Как же появилась выбранная хиральность в живых организмах?
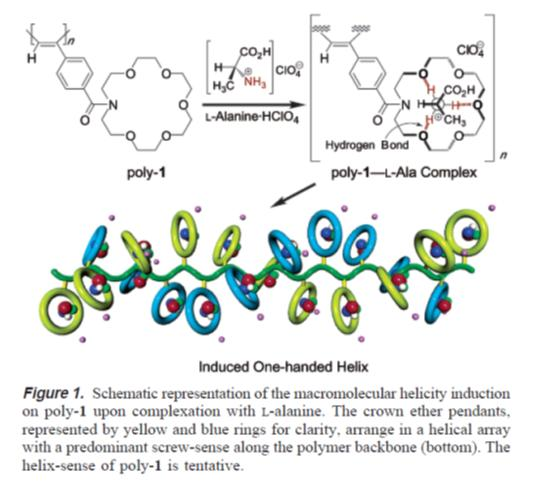
Рис. 2
В работах японских авторов обнаружен следующий удивительный эффект (рис. 2). Для определенных систем — комплекса полимерной молекулы и смеси низкомолекулярного хирального соединения в процессе комплексообразовании с одним оптическим изомером полимерная цепь сворачивается в правую (условно) спираль, при комплексообразовании с другим изомером — в левую. Однако самым удивительным оказалось, что если используется смесь изомеров с очень небольшим избытком одного из изомеров, то цепь сворачивается практически только в одну спираль, которая соответствует небольшому избытку изомера.
Возможным объяснением такого эффекта является необходимость наличия зародыша спирали большой длины для сворачивания всей макромолекулы. Соотношение вероятностей образования таких l и d-зародышей зависит в степенной степени от их длины (рис. 3).

Рис. 3
Поэтому небольшое различие в соотношении количеств изомеров приводит к значительной разнице вероятностей образования зародышей спирали – тем большей, чем длинней зародыш.
Эти рассуждения объясняют возможный механизм усиления незначительной случайной разницы в хиральности низкомолекулярных соединений, возникшей, например, при их синтезе. Главную роль в таком усиливающим эффекте играет полимерное состояние – не зря белки, ДНК, РНК и др. элементы живого являются высокомолекулярными соединениями.
- Как при высоких давлениях выход продукта зависит от деформации?
Авторы, изучающие химические реакции в твердой фазе при высоких давлениях и деформации сдвига на наковальнях Бриджмена (рис.4), обратили внимание на тот факт, что выход продукта зависит от угла поворота (сдвиговой деформации) практически независимо от скорости деформации, т.е. времени.
Другими словами, при построении кинетических кривых следует использовать координаты «выход – сдвиговая деформация» вместо привычных «выход – время». При сдвиговой деформации смеси двух твердых порошков поверхность раздела, вблизи которой идет их взаимодействие и образуется продукт, однозначно связана с величиной деформации (рис. 5). Поэтому и выход продукта зависит только от деформаций при отсутствии других диффузионных процессов, которые затруднены в твердой фазе. Очевидно, что и при проведении твердофазных химических реакций в других смесительных аппаратах (экструдеры, смеситель Брабендера и пр.) ситуация будет аналогичная, хотя и более сложная из-за неоднородности сдвиговых деформаций.
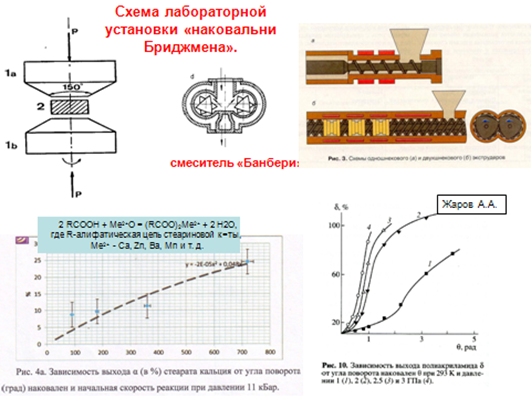
Рис. 4

Рис. 5
Следующие две загадки касаются стеклообразного состояния вещества, которое, несмотря на отсутствие дальнего порядка, проявляет часто те же макроскопические свойства, что и кристаллы, хотя объяснение этим свойствам для кристаллов дается с учетом дальнего порядка. Остановлюсь на двух явлениях: 1) переход твердое тело – жидкость и 2) пластическая деформация.
- Плавление и стеклование – различие и общее
Молекулярно-динамическое моделирование простых дисков и сфер позволяет наблюдать постепенный переход от кристаллического к стеклообразному состоянию. Для этого достаточно рассмотреть однородную смесь двух типов частиц разного диаметра. При увеличении относительной разницы диаметров система постепенно переходит от полностью упорядоченного кристалла (все частицы одинаковые) к неупорядоченному стеклообразному (при низкой температуре) состоянию. Нагревая эти системы, мы наблюдаем переход из твердого состояния в жидкое. При этом для одинаковых частиц и при небольшой разнице диаметров этот переход сопровождается скачком плотности (фазовый переход первого рода, плавление), а при большой разнице диаметров (больше некоторого критического значения) скачка плотности не наблюдается (размягчение стекла, стеклование при охлаждении). Важно отметить, что при этом фиксируется непрерывное снижение температуры перехода из твердого состояния в жидкое (рис. 6).
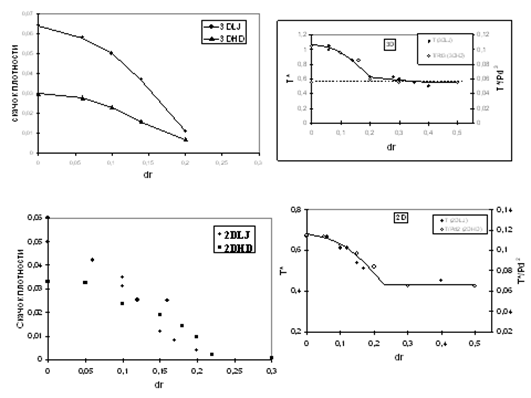
Рис. 6
Молекулярно-динамическое моделирование показало, что и плавление кристаллов, и размягчение (стеклование) стекла при увеличении температуры и соответственно объема происходит тогда, когда становится возможным обмен соседями. Простая модель из семи дисков на плоскости количественно подтверждает этот вывод (рис. 7). При дальнейшем увеличении температуры возникает самодиффузия и становится возможным протекание сдвиговой деформации без внешнего усилия.
Полученные результаты подтверждают общность между переходами кристалл-жидкость и стекло-жидкость. При этом различие этих переходов заключается в том, что в этой точке (температуре) при плавлении кристалла теряется дальний порядок и, следовательно, наблюдается скачок энтропии, а значит и энтальпии, что представляет собой фазовый переход первого рода. При размягчении стекла упорядоченность не меняется (дальнего порядка не было и в твердом стекле) и соответственно не наблюдается скачков энтропии и энтальпии (рис. 8).

Рис. 7
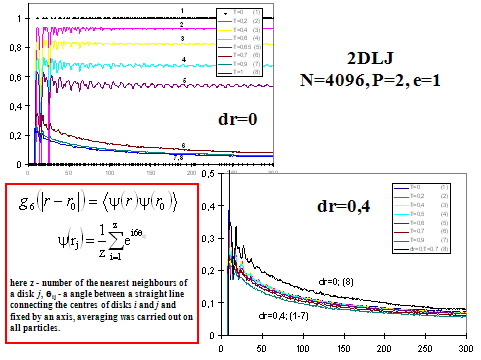
Рис. 8
- Пластическая деформация в стекле
Пластическая деформация кристаллических тел определяется наличием, размножением и движением дислокаций. В стекле нет дальнего порядка и нет дислокаций, но макроскопические проявления, такие как предел текучести и полосы сдвига, те же что и в кристаллах. Молекулярно-динамическое моделирование показало, что пластическая деформация в стеклах всегда сопровождается увеличением объёма, т.е. снижением плотности (рис.9).
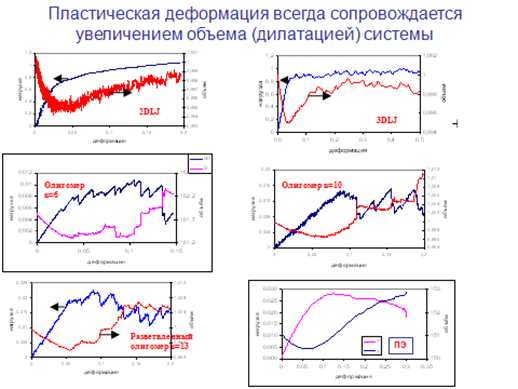
Рис. 9
Аналогичные результаты показывает и эксперимент. Заметим, что при деформации вблизи температуры стеклования происходит релаксация объёма, и экспериментально можно не заметить уменьшения плотности. Красивое доказательство роли снижения плотности было получено при моделировании процесса деформации твердых дисков и эллипсов на плоскости. В процессе деформации при переходе к пластическому течению (максимум на диаграмме сжатия δ-ε) появляются полосы сдвига (рис.10).

Рис. 10
При этом увеличивается объём (снижается плотность), уменьшается число контактов между твердыми частицами (рис.11), и именно в области полос сдвига частицы имеют малое количество контактов друг с другом и соответственно пониженную плотность (рис.12).
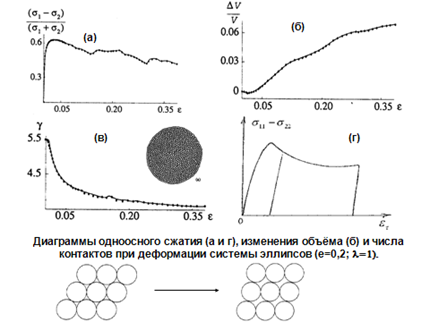
Рис. 11
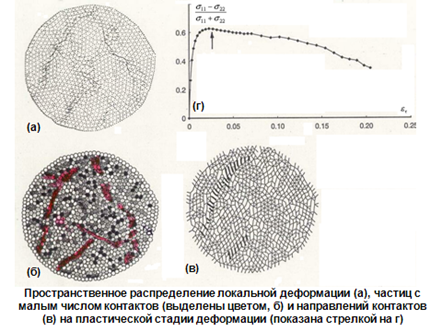
Рис. 12
Таким образом, можно сделать вывод, что в стеклах при сдвиговой деформации формируются зоны пониженной плотности, в которых облегчена деформация и которые аналогичны областям скопления дислокаций в кристаллических телах.
- Отрицательный коэффициент Пуанссона
Все обычные изотропные тела имеют положительный коэффициент Пуассона (рис.13), т.е. они расширяются в поперечном направлении при одноосном сжатии. Однако теория даёт возможность коэффициенту Пуассона (μ) изменяться от 0,5 до -1. Тело сохраняет свой объём при μ = 0,5 и свою форму при μ = -1.
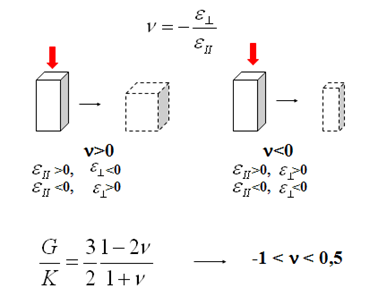
Рис. 13
Моделирование системы мягких сфер с двумя независимыми жесткостями в контакте частиц – нормальной и тангенциальной (рис.14) – показало, что величина μ=-1 может быть достигнута при условии значительного превосходства тангенциальной жесткости над нормальной. Все обычные потенциалы взаимодействия атомов друг с другом — центральные (тангенциальная жесткость существенно меньше нормальной) или близки к ним.
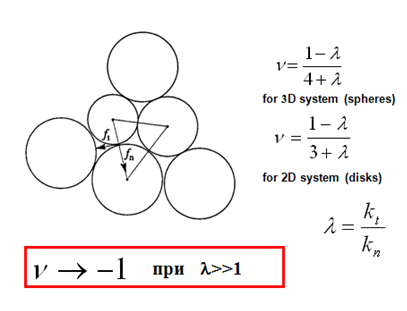
Рис. 14
Это могло бы оказаться чисто абстрактным рассуждением, если бы не экспериментальная работа американских авторов (рис. 15), в которой был синтезирован новый класс полимерных и металлических пен с отрицательным коэффициент Пуассона (μ ≈ -1). Метод получения такой пены состоял в следующем: обычную очень лёгкую полимерную или металлическую пену подвергали всестороннему сжатию и фиксировали в таком состоянии. При этом внутренние перегородки теряли устойчивость и изгибались. Такая изогнутая перегородка имеет тангенциальную жесткость больше, чем нормальная (рис.16).
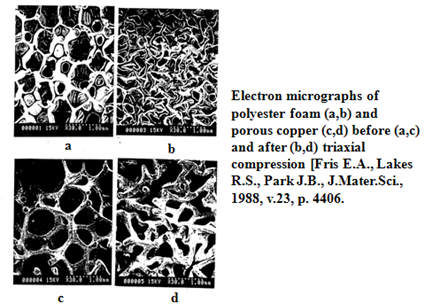
Рис. 15
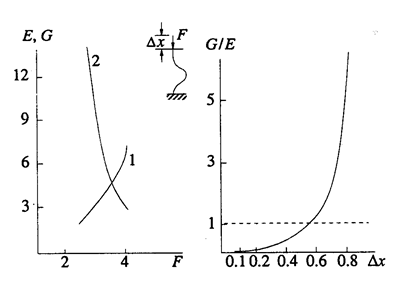
Рис. 16
Таким образом, для получения отрицательного коэффициента Пуассона необходимо создать структуру, узлы которой соединены потенциалом или элементами, имеющими большую тангенциальную и малую нормальную жесткость.
- Организация промышленных процессов химического производства
Принято считать, что при организации промышленных процессов следует стремиться к проведению химических реакций в «кинетическом» режиме. Приведем примеры, когда с точки зрения улучшения качества продукта и технологических параметров процесса выгоднее «диффузионный» режим.
Рассмотрим процесс полимеризации газообразного формальдегида в открытой системе.
Газообразный формальдегид подается в реактор с раствором катализатора, растворяется и полимеризуется в растворе (рис. 17).
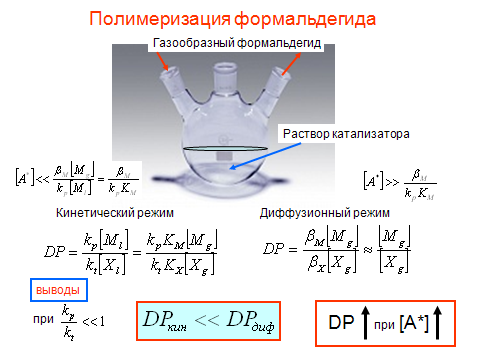
Рис. 17
В зависимости от условий (скорость подачи, скорость растворения, концентрация катализатора и пр.) возможны различные режимы химического процесса. Предельными режимами является «кинетический», когда скорость лимитируется скоростью самой химической реакции полимеризации, или «диффузионный», когда процесс лимитируется скоростью подвода мономера, т.е. либо подачей мономера в реактор или скоростью его растворения в жидкой фазе. Заметим, что критическим, определяющим качество полимера в данном случае является его молекулярный вес. В свою очередь, молекулярный вес определяется реакцией передачи цепи на примеси воды и метанола в формальдегиде. Поэтому необходимой и важной стадией производства полиформальдегида является его очистка от примесей. Рассмотрим два предельных случая.
- «Кинетический» режим. В этом случае концентрация формальдегида [Ф]ж и примеси [Пр]ж равна их растворимости в растворителе, а средняя степень полимеризации (и молекулярный вес соответственно) равна отношению скоростей роста и передачи цепи:
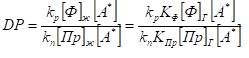 где [А*] — концентрация активных центров, КФ и КПр — константы растворимости формальдегида и примеси, [Ф]Г и [Пр]Г — концентрации формальдегида и примеси в газовой фазе.
где [А*] — концентрация активных центров, КФ и КПр — константы растворимости формальдегида и примеси, [Ф]Г и [Пр]Г — концентрации формальдегида и примеси в газовой фазе. - «Диффузионный» режим, при котором в реакцию полностью вступают поступающие в раствор из газовой фазы формальдегид и примесь. Тогда
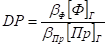 Отношения Кф/Кпр и βф/βПр не существенно отличаются от 1, в то время как отношение для катионной полимеризации формальдегида κp/κn<<1 . Именно поэтому молекулярный вес выше при проведении реакции в «диффузионном» режиме.
Отношения Кф/Кпр и βф/βПр не существенно отличаются от 1, в то время как отношение для катионной полимеризации формальдегида κp/κn<<1 . Именно поэтому молекулярный вес выше при проведении реакции в «диффузионном» режиме.
Еще один интересный и неожиданный результат – молекулярный вес полимера возрастает при увеличении концентрации катализатора, поскольку при этом происходит переход от «кинетического» к «диффузионному» режиму. Количественные критерии перехода: соотношения 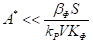 – «кинетический» и
– «кинетический» и 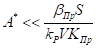 – «диффузионный» режимы.
– «диффузионный» режимы.
Здесь V – объём жидкости в реакторе, а S – поверхность, через которую идет растворение газов. Предполагается, что концентрации реагентов в жидкости постоянны по объёму, т.е. перемешивание жидкости происходит достаточно эффективно.
Промышленное крупнотоннажное производство – получение высокооктанового бензина, сернокислотное алкилирование изобутилена бутиленами является важным производственным процессом. И в этом случае «диффузионный» режим оказывается полезным, а схема реакции представлена ниже.
Общепринято, что каталитическое алкилирование изоалканов идет через промежуточное образование ионов карбония:![]()
Вторичный ион карбония менее устойчив, чем третичный, вследствие чего происходит быстрый обмен гидрид-ионом с изопарафином:![]()
Образующийся третичный карбоний-катион реагирует с исходным олефином: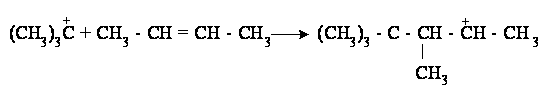
Получившийся ион карбония склонен к внутримолекулярным перегруппировкам, сопровождающимися миграцией водорода и метильных групп.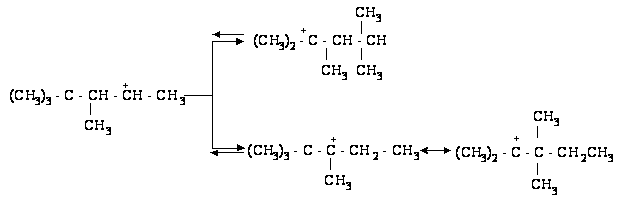
Ионы карбония взаимодействуют с изобутаном, в результате чего получается С8Н18 и третичный бутил-катион: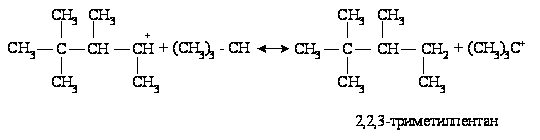
Таким образом, образуются изомерные углеводороды C8H18, представляющие собой основной и наиболее ценный продукт. Кроме того, процесс сопровождается протеканием побочных реакций:![]()
![]()
и т.д., приводящих к получению ненасыщенных полимеров, ухудшающих качество алкилата и ведущих к повышенному расходу катализатора.
Применение избытка изоалканов подавляет все побочные реакции, положительно влияет на выход и качество алкилата, повышает его октановое число, снижает расход катализатора и себестоимость продукта.
Оказалось, однако, что если подавать вначале серную кислоту с изобутаном, создавая эмульсию, в которой кислота диспергирована в изобутане, либо изобутан в кислоте, а только потом бутилены, как это показано на рис. 18б, то существенно уменьшается количество побочных продуктов и расход кислоты (меньше образуется кислого гудрона) и улучшается качество продукта (значительно повышается октановое число).
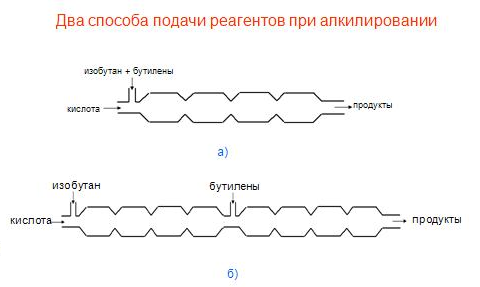
Рис. 18
Какова же причина наблюдаемого явления?
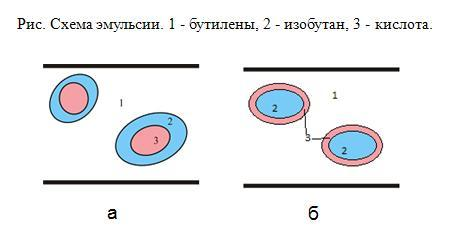
Рис. 19
Объяснение может заключаться в следующем: после смешения кислоты с изобутаном получается эмульсия либо кислота-изобутан (рис. 19а), либо изобутан-кислота (рис. 19б). Эта эмульсия попадает в среду бутиленов и они начинают растворяться в изобутане и/или в кислоте. Диффузия в первом случае идет с поверхности мицеллы, и концентрация бутиленов у поверхности кислоты мала. Таким образом, реакция протекает в избытке изобутана, что и требуется для получения качественного продукта (алкилата) и снижения расхода кислоты (уменьшения количества кислого гудрона). В этих условиях нет необходимости создавать большой переизбыток изобутана. Необходимым критерием осуществления данного процесса, протекающего при низкой концентрации бутиленов в зоне химической реакции, является сравнительно медленная диффузия бутиленов в изобутане по сравнению со скоростью самой реакции алкилирования или, где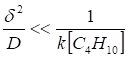 где
где ![]() — характерное время диффузии; δ — толщина пленки изобутана; D – коэффициент диффузии бутилена в изобутане;
— характерное время диффузии; δ — толщина пленки изобутана; D – коэффициент диффузии бутилена в изобутане; 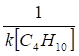
— время химической реакции; k – эффективная константа скорости бимолекулярного процесса превращения бутилена на границе раздела фаз кислота-изобутан.
Таким образом, переход в диффузионную область позволяет обеспечить в области химической реакции (вблизи поверхности серной кислоты) большой избыток изобутана, хотя в среднем (по всему объему) это может быть и не так.
Таким образом, при полимеризации формальдегида «диффузионный» режим позволяет увеличить молекулярный вес продукта. При сернокислотном алкилировании изобутана бутиленами в «диффузионном» режиме повышается выход продукта, октановое число и уменьшается расход катализатора.
- История получения полиформальдегида
История получения полиформальдегида полимеризацией циклического тримера формальдегида триоксана начиналась с загадки. Были обнаружены высокие порядки скоростей полимеризации в зависимости от концентрации триоксана (вплоть до 7), несвязанные с диэлектрической постоянной или другими физико-химическими свойствами растворителя (рис. 20).
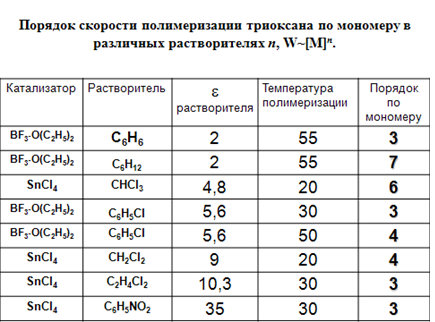
Рис. 20
В ряде случаев (например, в н-гептане и циклогексане) наблюдалась аномальная экстремальная (с максимумом и минимумом) зависимость выхода полимера от концентрации мономера (рис. 21). Оказалось, что решение этих загадок лежит в гетерогенном и обратимом характере полимеризации триоксана (рис. 22). Наличием двух типов активных центров — растворенного и «твердого» (находящегося на поверхности твердого полимера), их превращением друг в друга за счет кристаллизации полимера и различием по термодинамическим и кинетическим параметрам удалось объяснить все удивительные особенности кинетики (рис. 23,24).
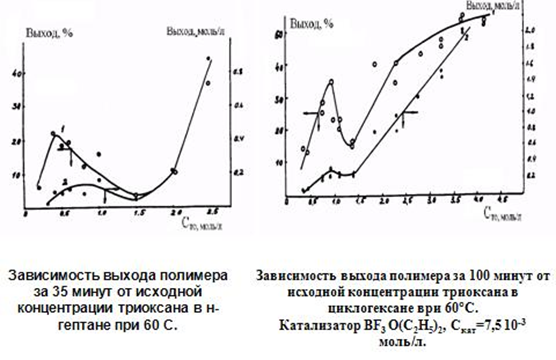
Рис. 21
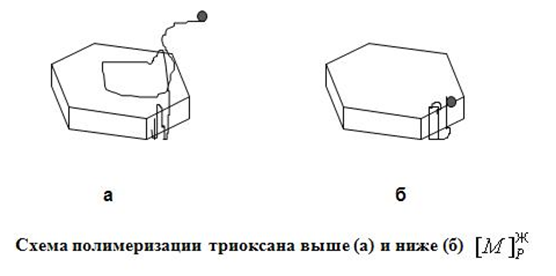
Рис. 22
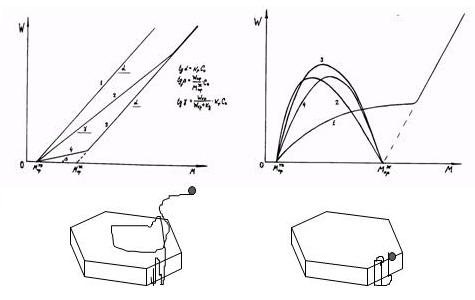
Рис. 23
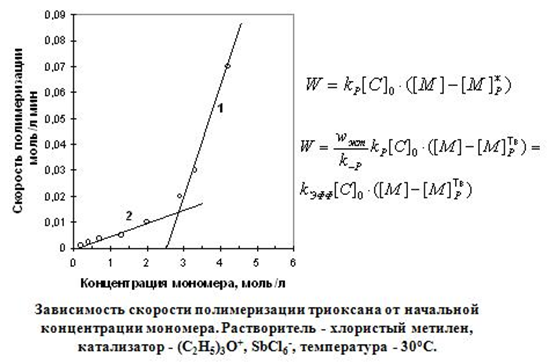
Рис. 24
Кроме того, структура образующегося полимера существенно зависит от условий полимеризации. Так проведение реакции при низких концентрациях мономера, т.е. тогда, когда процесс термодинамически возможен только благодаря выпадению в твердую фазу, и реакция протекает на активных центрах, расположенных на твердой поверхности полимера, приводит к получению крупных полимерных кристаллов. При высоких же концентрациях мономера полимеризация идет на растворенных активных центрах, а затем полимер выпадает в осадок в виде мелких неоформленных частиц (рис. 25).
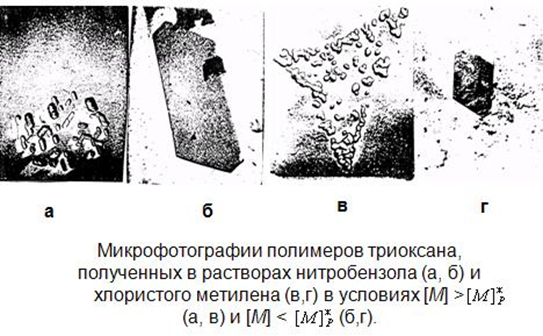
Рис. 25
В этой связи возникла идея термодинамического регулирования структуры (в том числе и молекулярной) полимера (рис. 26). В частности, было показано, что состав сополимера триоксана и диоксалана совершенно различен при полимеризации, протекающей выше и ниже предельной равновесной концентрации триоксана по отношению к растворенному полимеру. При высоких концентрациях триоксана наблюдается обычная зависимость состава полимера от состава мономерной смеси при примерно равных константах сополимеризации (рис. 27).
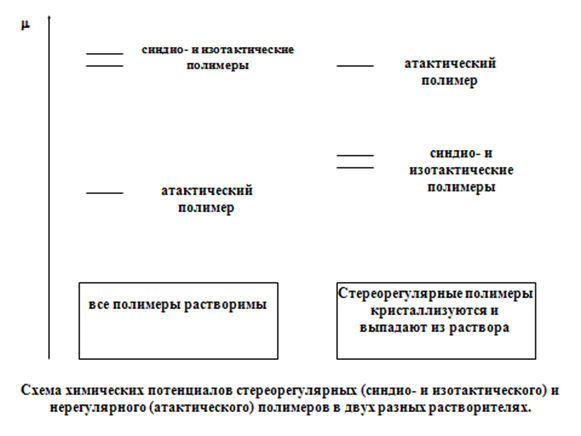
рис. 26
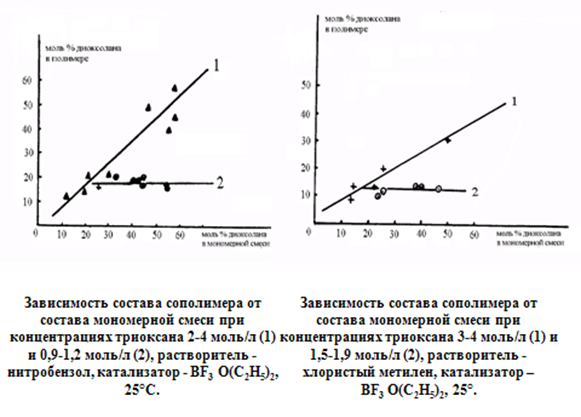
Рис. 27
При низких концентрациях триоксана образуется полимер в виде крупных кристаллов одного и того же состав независимо от состава мономерной смеси (рис. 28).
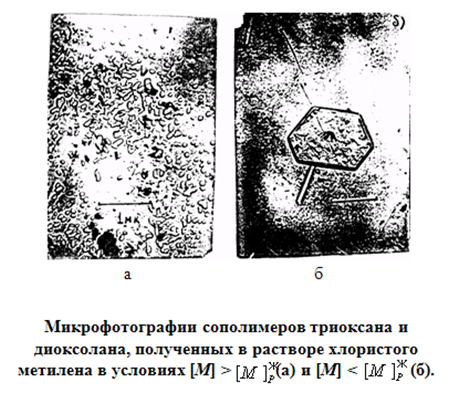
Рис. 28
Литература к разделам
- А.А. Берлин, Н.А. Халтуринский, А.Ю. Шаулов. Полимерные материалы пониженной горючести. // Горение и плазмохимия. 2006. Т. 4. № 2. С. 79-88.
- Ал.Ал. Берлин. Горение полимеров и полимерные материалы пониженной горючести // Соросовский образовательный журнал. 1996. № 9. С. 57.
- В.А. Аветисов, академик А.А. Берлин, В.В. Иванов. О механизме высокой чувствительности спирализации полифенилацетилена с краун эфирными пендантами к малому энантиомерному избытку аминокислот. // ДАН. 2004. Т. 395. № 4. С.1-3.
- Nonokawa R. and Yashima E. // J. Am. Chem. Soc. 2003. V. 125. P. 1278-1283.
- Yashima E., Maeda K., Okamoto Y. // Nature. 1999. V. 399. P. 449-451.
- Ishikawa M., Maeda K., Yashima E. // J. Am. Chem. Soc. 2002. V. 124. P. 7448-7458.
- Brunsveld L., Folmer B. J. B., Meijer E. W., Sijbesma R. P. // Chem Rev. 2001. V. 101. P. 4071-4097.
- Green M. M. et al. // Science. 1995. V. 268. P. 1860.
- Ал.Ал. Берлин. Об одной простой интерпретации кинетики быстрых твердофазных реакций. // Химическая физика. 2018 (в печати).
- А.А. Жаров. // Высокомолек. соед. Б. 2004. Т. 46. №9. С. 1613-1637.
- Berlin Al.А, Gendelman О.V., Sinelnikov N.N., Маzо М.А., Маnevich L.I. On solid-liquid transition in plane disk systems. // Journal of Physics: Condensed Matter. 1999. V. 11. № 24. Р. 4583-4596.
- Berlin Al.А, Gendel’man О.V., Sinel’nikov N.N., Mazo М.А., Manevich L.I. An Analysis of the Structure and Thermodynamic Properties of Bicomponent Systems of Disks and Spheres. // Russian J. Phys. Chem. 2000. V. 74. suppl. 1. (only in English) P. 46-51.
- Берлин Ал.Ал., Гендельман О.В., Мазо М.А., Маневич Л.И., Балабаев Н.К. Плавление кристаллов из упругих и леннард—джонсовых сферических частиц. // ДАН. 2002. Т. 382. № 6. С. 798-801.
- Берлин Ал.Ал., Мазо М.А. Плавление и стеклование смесей леннард-джонсовых сфер. // Все материалы. Энциклопедический справочник .«Наука и технологии» 2012. № 8. С. 2-6.
- Berlin Al.А, Mazo М.А. Melting and Vitrification of Lennard_Jones Spheres // Polymer Science, Series D. Glues and Sealing Materials. 2013. V. 6. №. 3. Р. 228-231.
- Берлин Ал.Ал., Ротенбург Л., Басэрст Р. Деформационное поведение и переход стекло — жидкость в гранулированных системах. // Химическая физика. 1991. Т.10. № 9. С. 1284-1291.
- Берлин Ал.Ал., Ротенбург Л., Басэрст Р. Особенности деформации неупорядоченных полимерных и неполимерных тел. // Высокомолек. соед. А. 1992. Т. 34. № 7. С. 6-32.
- Берлин Ал.Ал., Мазо М.А., Балабаев Н.К. Природа дефектов, возникающих при пластической деформации стекол. // Все материалы. Энциклопедический справочник «Наука и технологии» 2012. № 10. С. 10-13.
- BerlinАl., Mazo M.A., Strel’nikov I.A., Balabaev N.K. Modeling of plastic deformation of glasses in creeping and stress relaxation regimes. // Polymer Science. D. April 2015. V. 8. № 2. P. 85-91.
- Berlin Al.Al., Rothenburg L., Bathurst R.J. Mechanics of disordered glass-like body. // 3-rd Japan — USSR Joint Symposium on Advanced Composite Materials. Moscow. USSR. 1991. Р. 319-345.
- Rothenburg L., Berlin Al.Al., Bathurst R.J. Microstructure of isotropic materials with negative Poisson’s ratio // Nature. V. 354. № 6353. Р. 470-472.
- Берлин Ал.Ал., Ротенбург Л., Басэрст Р. Структура изотропных материалов с отрицательным коэффициентом Пуассона // Высокомолек. соед. Б. 1991. Т.32. № 8. С. 619-625.
- Берлин Ал.Ал., Вольфсон С.А. Кинетический метод в синтезе полимеров. Москва. Химия. 1973.
- Берлин Ал.Ал., Вольфсон С.А., Ениколопян Н.С., Кинетика полимеризационных процессов. Москва. Химия. 1978.
- Ал.Ал. Берлин, Н.С. Ениколопян, Термодинамика и кинетика обратимой полимеризации в присутствии твердого полимера. // Высокомолек. соед. А. 1969. Т. № 12. С. 2671.
- Ал.Ал .Берлин, К.А. Богданова И.П. Кравчук, Г.В. Ракова, Н.С. Ениколопян. О равновесном характере полимеризации триоксана // Докл. АН СССР. 1969. Т. 184. № 5. С. 1128.
- Ал.Ал. Берлин, С.А. Вольфсон, Э.Ф. Олейник, Н.С. Ениколопян, Термодинамика равновесия формальдегид-триоксан-поли-формальдегид // Высокомолек. соед. А. 1970. Т. 12. № 2. С. 443.
- Ал.Ал. Берлин, Г.А. Карюхина, Г.М. Трофимова, Н.С. Ениколопян, О надмолекулярных структурах при равновесной полимеризации триоксана // Докл. АН СССР. 1970. Т. 195. № 5. С. 1147.
- Ал.Ал. Берлин, Н.С. Ениколопян, Термодинамические основы регулирования структур полимеров при их образовании // Докл. АН СССР. 1971. Т. 196. № 5. С. 1111.
- Ал.Ал. Берлин, К.А. Богданова, Г.В. Ракова, Н.С. Ениколопян. О равновесии в системе триоксан-тетраоксан-полиоксиметилен // Высокомолек. соед. А. 1972. Т. ХIV. № 9. С. 1976.
- Ал.Ал. Берлин, И.П. Кравчук, Г.В. Ракова, Б.А. Розенберг, Н.С. Ениколопян. О механизме обратимой гетерогенной полимеризации триоксана в растворе // Высокомолек. соед. А. 1973. Т. XV. № 3. С. 554.
- Ал.Ал. Берлин, К.А.Богданова, М.А. Маркевич, Г.В. Ракова, Н.С. Ениколопян. Термодинамические характеристики равновесия триоксан тетраоксан-формальдегид-поли-оксиметилен в гомогенных условиях // Докл. АН СССР. 1973. Т. 211.№ 4. С.874.
- Ал.Ал. Берлин, Г.А. Воробьева, Г.М. Трофимова, Н.С. Ениколопян. Термодинамический подход к регулированию надмолекуляр-ных и молекулярных структур полимеров // Высокомолек. соед. А. 1974. Т. XVI. № 7. С. 1493.
- Ал.Ал. Берлин, Г.А. Воробьева, Г.М. Трофимова, Н.С. Ениколопян, Исследование надмолекулярных структур полипиперазина, образующихся в ходе полимеризации триэтилендиамина // Докл.АН СССР. 1974. Т. 214. № 2. С. 373.
- Ал.Ал. Берлин, К.А. Богданова, Г.В. Ракова, Н.С. Ениколопян. Термодинамические параметры образования полиоксметилена // Высокомолек. соед. А. 1975. Т. XVII. № 3.С. 643.
- Ал.Ал. Берлин, К.А. Богданова, В.З. Компаниец, Г.В. Ракова, Е.А. Мирошниченко, Ю.А. Лебедев Н.С. Ениколопян Об энтальпиях гомогенной полимеризации триоксана и тетраоксана // Высокомолек. соед. А. 1975. Т. XVII. № 3. С.658.
- Ал.Ал. Берлин, Р.Я. Дебердеев, Ю.В. Перухин, Р.М. Гарипов, Влияние термодинамических условий полимеризации на надмолекулярную и молекулярную структуру полимеров // Клеи. Герметики. Технологии. ООО «Наука и технологии». 2009. № 2. С. 2-7.